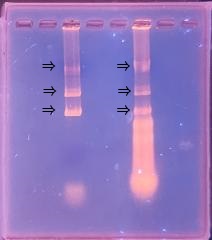
1年生の微生物学実習で腸内細菌の同定を行いました。
1晩培養した確認培地を観察していよいよ判定です。
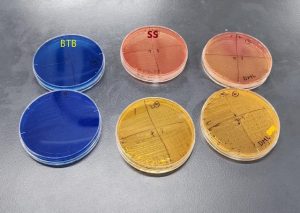
TSI培地はtriple sugar iron寒天培地といい、
斜面部で乳糖、白糖の分解、
高層部でブドウ糖の発酵、ガスの産生、硫化水素の産生を見ることができます。
一番左が菌を植える前です。(これ以降の培地すべて)
糖を分解すると酸を産生するので培地が黄色に変化します。
ガスが産生すると培地に亀裂が入ったり、培地が浮いたりします。
硫化水素を産生すると培地が黒変します。
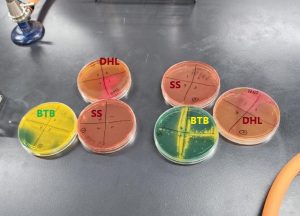
SIM培地は硫化水素の産生、IPA反応、インドールの産生、運動性、が見られます。
シモンズクエン酸培地は炭素源としてクエン酸ナトリウム、
窒素源としてアンモニウム塩のみを含む合成培地です。
これらを利用できる菌のみが発育でき、
発育すると培地は緑色から青色(アルカリ性)に変化します。
VP半流動培地はアセチルメチルカルビノール(アセトイン)の生成が確認できます。
VP試薬を加えて混和し、赤色に変化したら陽性です。
チトクロームオキシダーゼ試験で好気性菌と通性嫌気性菌の鑑別も行いました。
これらの結果を総合して未知検体を同定します。
今回は大腸菌、肺炎桿菌、サルモネラ、プロテウスの4つの菌から2つを同定しました。
上手く同定できたのでしょうか。。。
細菌にもいろいろな性状がありますね。
それらを調べるためにいろいろな培地が開発されていますね。