みなさん、こんにちは。
2年生の生化学実習も最後の実技試験を残して、
今回が最後の実習です。
今回の実習は、糖の定性試験を行いました。
まずは、使用する試薬の調製からです。
協力して調製していきます。
試薬調製後、いよいよ定性試験です。
今回使用する糖は、
キシロース、グルコース、フルクトース、
マルトース、ショ糖、デンプン、
そして対象として、
水の7種類について定性試験を行いました。
番号順が逆ですが、すみません。
7本の試験管にいずれかの糖が入っています。
定性試験により同定していきます。
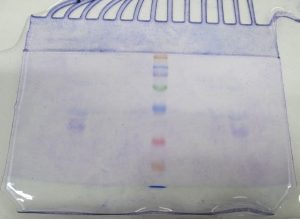
それでは、定性試験の結果を見ていきましょう。
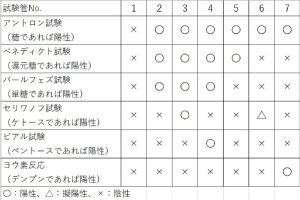
アントロン試験(糖であれば陽性)の結果です。
糖であれば青緑色になります。
水は糖ではありませんので反応しません。
No.1は反応してないようです。
ベネディクト試験(還元糖であれば陽性)の結果です。
還元糖は赤色沈殿ができます。
No.2、3、4、5に赤色沈殿があるようです。
バールフェズ試験(単糖類であれば陽性)の結果です。
単糖類であれば赤色沈殿ができます。
No.2、3、4に赤色沈殿があるようです。
No.7は白く濁っています。
セリワノフ試験(ケトースであれば陽性)の結果です。
ケトース(ケト基をもつ単糖類)であれが紅色になります。
No.3、6が紅色になったようです。
ビアル試験(ペントースであれば陽性)の結果です。
ペントース(五炭糖)であれば青緑色になります。
No.4が青緑色になったようです。
最後にヨウ素反応(デンプンであれば陽性)の結果です。
デンプンであれば青紫色になります。
No.7が青紫色になったようです。
以上、6種類の定性試験を行い、
試験管7本の同定を行いました。
写真では少しわかりずらいので、
一覧表にしてみました。
一覧表をもとに、
みなさんも同定をしてみてください。
今回使用した糖類です。
単糖類(キシロース、グルコース、フルクトース)、
二糖類(マルトース、ショ糖)、
多糖類(デンプン)、
水
補足:還元性有(単糖類とマルトース)、
ケトース(フルクトース)、
ペントース(キシロース)
みなさん、いかかですか。
7本の試験管を同定できましたか。
それでは答え合わせです。
No.1(水)、
No.2(グルコース)、
No.3(フルクトース)、
No.4(キシロース)、
No.5(マルトース)、
No.6(ショ糖)、
No.7(デンプン)となります。
ショ糖は、フルクトース(ケトース)を含んでいますので、
セリワノフ反応で擬陽性を示します。
2年生のみなさん、次回は実技試験です。
頑張っていきましょう。